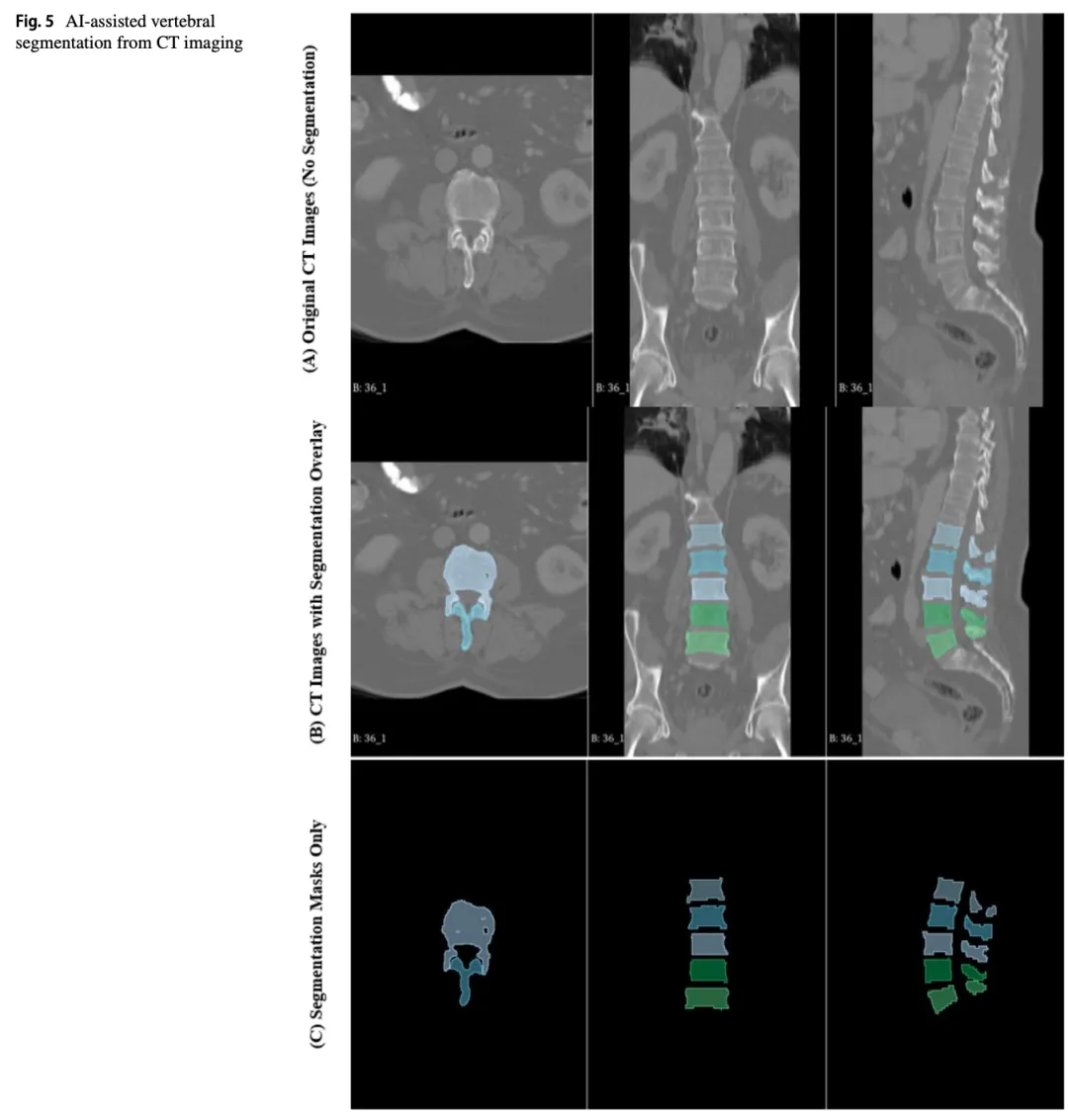
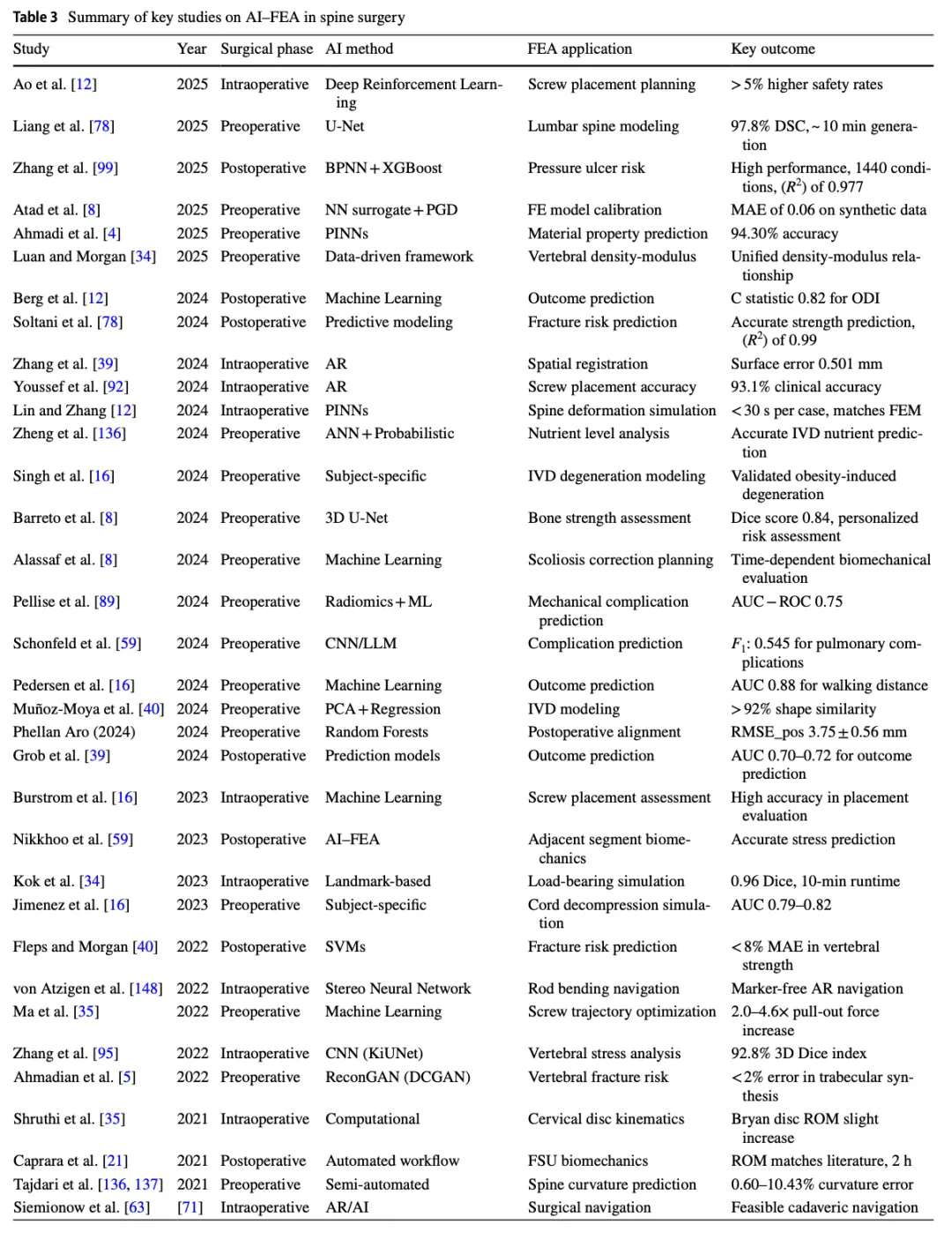
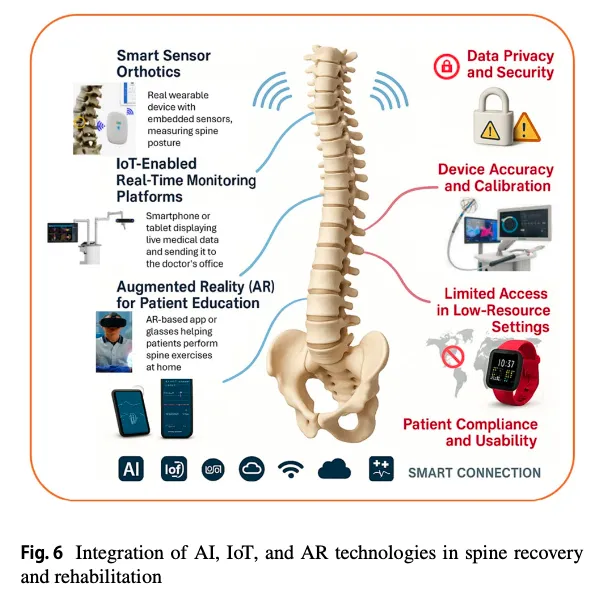
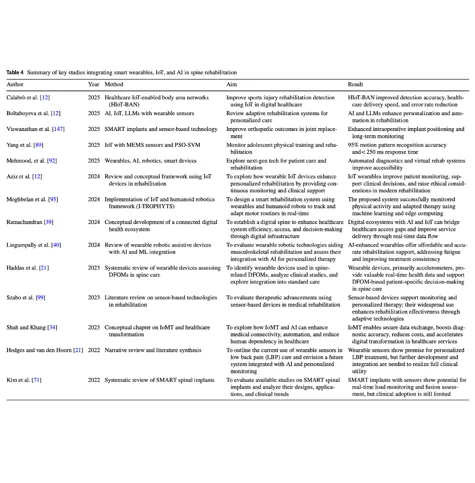
AI结合有限元将是生物力学研究的下一个重要风口!2025年脊柱生物力学综述
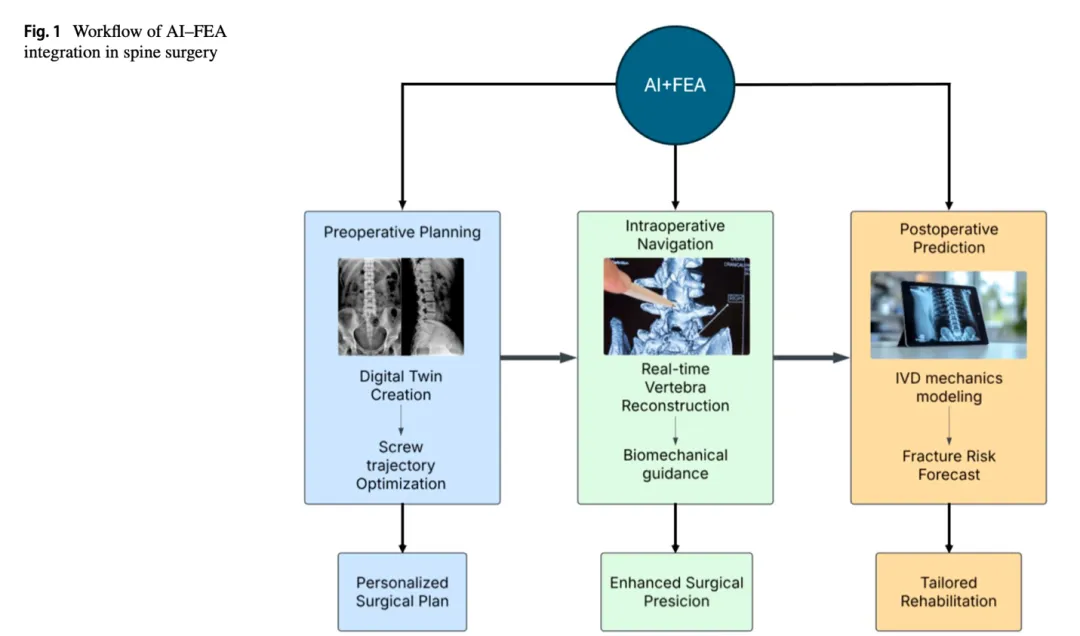
有限元分析技术在骨科生物力学研究中是曾经的经典方法,但因为建模操作繁琐,计算量大,数据验证困难,目前只是科研水论文的好技术,连内植物产品注册检验都无法应用有限元数据,更未推广到临床。AI技术发展给有限元的推广产生了希望,如此基于力线的手术理念将走向下一个的基于力学平衡手术理念,这里仍重而道远。 新兴的AI-FEA 融合如何革新脊柱手术 Franceschini C, Ahmadi M, Zhang X, Wu K, Lin M, Weston R, Rodio A, Tang Y, Engeberg E, Pires G, Cheema TS, Vrionis FD. Revolutionizing spine surgery with emerging AI-FEA integration. J Robot Surg. 2025 Sep 18;19(1):615. doi: 10.1007/s11701-025-02772-w. PMID: 40965805; PMCID: PMC12446114. 摘要 本研究探讨了人工智能(AI)与有限元分析(FEA)在脊柱手术中的融合应用,重点阐述了它们在术前规划、术中执行和术后结果预测中的互补作用。AI和 FEA 的协同作用正在通过改进生物力学建模、增强手术精准度和实现个性化治疗策略,重塑现代脊柱外科。在术前阶段,AI增强的 FEA 支持个性化手术方案的设计,优化植入物放置,并模拟各种负荷条件下的力学响应。术中,AI能够实现实时图像引导导航、机器人辅助和自动化解剖结构识别,从而降低手术错误风险。术后,基于FEA 模拟和患者数据的预测模型有助于跟踪康复进程、预测并发症并指导康复方案。这些技术共同推动了脊柱外科向数据驱动的精准医学范式转变。随着智能反馈系统、数字孪生体和自主手术平台的不断发展,AI-FEA融合有望在提供更安全、更高效、更个体化的脊柱治疗中发挥变革性作用。 关键词人工智能·有限元分析·脊柱外科·数字孪生·手术规划·术中导航·术后预测 引言 脊柱疾病是一项重大的全球健康挑战,影响约4.9% 的人口,且在女性中患病率更高[12]。这些疾病是全球范围内导致残疾的主要原因之一,并贡献了相当部分的医疗资源消耗。所有医疗转诊中的25%–30% 以及全球约15% 的病历认证与脊柱病变相关,仅在美国每年的相关费用就超过1000 亿美元 [71]。随着人口老龄化和预期寿命延长,这一负担预计将进一步加重,尤其影响低收入地区的男性和老年人。脊柱疾病的谱系,包括退行性椎间盘疾病、脊柱侧凸、脊髓损伤和复杂畸形,带来了多样的诊断和治疗挑战[40]。此外,社会经济差异、资源匮乏地区手术专业知识的缺乏以及康复服务的不平等获取,进一步使治疗结果复杂化[16]。 在过去的几十年里,脊柱外科经历了重大转变,从侵入性、通用型手术转向更精细、个体化的干预。术中成像、机器人辅助和实时手术导航等创新技术显著提高了手术安全性,减少了软组织损伤并加速了康复[119]。微创技术,例如微创经椎间孔腰椎椎体间融合术(MIS-TLIF),与传统开放TLIF 相比显示出显著优势,包括减少术中出血和缩短住院时间[131]。与此同时,骨科材料科学的进步进一步改善了手术效果。钛和不锈钢等金属因其强度和生物相容性仍被广泛使用;然而,对炎症和离子浸出的担忧促使了聚合物(如聚醚醚酮PEEK 和聚乳酸 PLA)在固定装置和椎间融合器中的应用[27, 115, 144]。这些材料是透射线的,减少了随访期间的成像伪影,并提供更接近天然骨的力学性能。此外,陶瓷和生物可吸收材料提供了更多选择,具有更好的骨整合能力和可定制的生物力学行为[142]。尽管这些创新显著推进了脊柱治疗,但人工智能(AI)和基于物理的生物力学模拟(特别是有限元分析FEA)的融合代表了下一个前沿。这些新兴工具有望实现更个性化、可预测和高效的手术规划及治疗结果。 人工智能在脊柱外科中的前景 人工智能(AI),特别是通过机器学习(ML)和深度学习(DL),正迅速成为现代医疗保健中的变革力量。在脊柱外科,毫米级的精准度可对患者结局产生关键影响,AI在导航脊柱复杂解剖结构方面提供了显著优势。它在医学影像解读、疾病分类、结果预测和术中指导方面展现出强大性能[1, 12]。AI 在脊柱治疗中广泛应用的初始障碍,如数据稀缺、成像方案差异和脊柱解剖的复杂性,已逐渐被克服。值得注意的是,约86% 的脊柱相关 AI论文发表于2017 年之后,表明该领域呈指数级增长[34]。表 1 提供了人工智能在脊柱外科不同阶段主要应用的结构化概述。它将AI 实施分为四个关键手术阶段:诊断、术前规划、术中执行和术后监测,突出了AI 技术(特别是卷积神经网络CNN 和增强现实 AR)如何改变临床工作流程。 神经网络,尤其是卷积神经网络(CNN),已被证明能够在MRI 和 CT 扫描中高精度地检测椎管狭窄、骨折、肿瘤和椎间盘退变[6, 40]。AI 在脊柱外科中的应用大致可分为四个阶段:(1)诊断,包括脊柱病理的检测和疾病严重程度分级;(2)术前规划,AI模拟最佳螺钉轨迹并推荐手术策略[35, 78];(3)术中执行,通过机器人和增强现实工具提高精准度[7];(4)术后监测,AI模型帮助追踪康复进程并制定个性化康复方案。 有限元分析(FEA)一直是脊柱生物力学的基础。通过将脊柱解剖结构分解为离散单元的网格,FEA能够计算各种生理和病理载荷条件下的应力、应变和位移[34]。其应用范围从植入物测试到手术模拟和材料评估。然而,传统的FEA 耗时、计算量大,并且依赖于分割、网格划分和属性分配等人工步骤[34],这使其在快节奏的临床环境中不切实际。AI与 FEA 的融合解决了这些问题。AI可以自动化几何分割、优化网格生成并预测材料属性,从而实现更快、更个性化的建模[4, 39]。一个重要的进展是物理信息神经网络(PINN)的使用,它将生物力学方程嵌入到网络结构中,实现了数据驱动和物理驱动的模拟。这在估算脊柱负荷、椎间盘退变行为和手术结果方面尤为有用。AI不仅正在革新脊柱外科,也在改变医学的多个领域。 传统植入物是基于通用解剖数据进行批量制造的。虽然功能正常,但这种方法通常无法适应患者特定的几何形态,导致对线问题和康复时间延长[90]。增材制造(3D打印)允许快速原型制作和生产针对个体患者的植入物[101]。钛、PEEK 和混合复合材料等材料正被用于制造具有高力学保真度的椎体融合器、椎弓根螺钉和人工椎间盘[45, 156]。生物打印(使用载有细胞的生物墨水)也正在探索用于再生椎间盘和椎间组织。AI通过优化设计参数(如孔隙率、刚度梯度和骨小梁结构)为3D 打印做出贡献[10]。当与患者特异性成像和FEA 相结合时,这些技术能够实现完全定制的解决方案。近期研究将AI 在脊柱中的应用分为六个临床领域[34]。图 1 展示了AI-FEA 整合在脊柱手术连续过程(术前、术中和术后阶段)中的工作流程,重点介绍了数字孪生创建、实时导航和骨折风险预测等关键应用。使用Lucid (lucid.co) 创建。AI 通过自动化耗时的任务(例如从成像数据生成患者特定模型)以及优化模拟以预测生物力学结果(如脊柱稳定性或植入物性能)来增强FEA。例如,AI 可以简化针对个体解剖结构定制的手术方案设计,与传统方法相比,提高了精确度并降低了风险。图1 展示了这一工作流程,强调了AI-FEA 如何在各个阶段协作以改善结果[59, 99]。 AI 在脊柱成像和手术规划中的应用已扩展到六个关键临床领域。首先,图像改进技术提高了CT 和 MRI 分辨率,同时减少了所需的辐射剂量,使成像更安全、更高效。其次,AI通过准确检测脊柱弯曲异常、椎体骨折和植入物来支持诊断。第三,在疾病分级中,AI模型以高精度协助临床医生对椎管狭窄、椎间盘退变和后纵韧带骨化(OPLL)等状况进行分类。第四,手术模拟能力使AI 能够推荐最佳螺钉轨迹,甚至为规划和培训目的生成合成CT 图像。第五,AI实现了机会性诊断,即分析常规影像以发现可能被忽视的隐匿风险因素,如骨密度低或肌肉退变。最后,在决策支持方面,AI系统预测潜在的术后并发症并帮助设计个性化治疗方案,有助于实现更知情、个性化和数据驱动的脊柱治疗。 脊柱治疗正朝着由连续数据流驱动的智能系统发展。数字孪生(患者解剖结构的实时计算模型)将允许对手术结果和康复进行动态模拟[16]。大型语言模型(LLM)正被整合到手术支持系统中,用于生成临床报告和分诊响应[34]。像 PINN 这样的物理信息模型将进一步弥合生物力学现实与学习效率之间的差距,减少对大型数据集的依赖。同时,可解释的AI(XAI)将使模型输出透明且可信,促进临床采用[1, 131]。 挑战与贡献 尽管取得了有希望的进展,挑战依然存在。目前尚无普遍接受的数据集用于训练脊柱成像或生物力学AI,导致可重复性问题。许多工具仍处于实验阶段,未获FDA 批准用于临床[12]。伦理问题包括数据偏见、隐私风险和AI 建议的透明度。此外,先进的3D 打印材料需要在活体条件下进行长期验证[115]。在资源匮乏环境中实现公平可及性也是一个重大挑战。本综述对AI-FEA 在现代脊柱外科中的作用进行了全面、多学科的综合分析。主要贡献包括: 我们旨在为未来智能脊柱治疗提供路线图,将临床精准度与计算智能相结合。本文面向研究人员、临床医生和技术专家,旨在减少并发症、降低成本并改善脊柱外科的结局。 脊柱外科中的AI-FEA 协同 AI 和 FEA 的融合正在通过提供更精确、数据驱动的手术规划和生物力学评估方法,彻底改变脊柱外科。FEA长期以来一直是分析脊柱组件如何响应各种力学力的基础方法。然而,开发FEA 模型的传统工作流程(例如手动分割CT/MRI 数据、创建网格和分配材料属性)耗时且通常需要专家输入[4]。AI 通过深度学习模型简化并增强了这一过程,这些模型可以自动化解剖分割、预测患者特异性生物力学属性并生成高质量的计算网格[78]。这种协同作用带来了更快、更个性化的模拟,支持临床医生规划复杂的干预措施,如脊柱畸形矫正或椎间盘假体植入。人工智能和机器学习正在重塑脊柱研究和实践。Galbusera等人 [21] 回顾了它们的应用,从图像分割和计算机辅助诊断到生物力学和结果预测,为其与有限元分析的整合以优化手术结果奠定了基础。AI-FEA之间的协作通过在所有手术阶段(术前规划、术中执行和术后恢复)实现个性化、数据驱动的干预,彻底改变了脊柱外科[35]。 图 2 展示了脊柱外科中AI-FEA 之间的协同联系。 表 2 手术中的 AI(AI in S)与人工智能手术(AIS)的比较 除了术前建模,AI与 FEA 的整合将其优势扩展到术中指导和术后结果预测。通过利用AI 从大型数据集中学习的能力和FEA 模拟真实力学行为的能力,这些混合模型可以预测手术结果,如植入物稳定性、应力分布和愈合潜力。像物理信息神经网络(PINN)这样的先进AI 技术尤其有前景,因为它们可以用最少的训练数据推断复杂的材料行为并模拟脊柱生物力学[4]。这使得创建实时模拟来指导手术决策成为可能,为个性化手术提供了一种“虚拟原型设计”形式[21]。 随着AI-FEA 整合的不断成熟,它正在将脊柱外科转变为一个更具预测性和患者特异性的学科。外科医生现在可以在反映患者解剖结构和病理的虚拟脊柱模型上评估多种手术策略,最终降低术中风险并改善术后结果。 例如,通过 AI增强的 FEA 开发的模型已用于预测假关节风险、优化螺钉轨迹和评估融合质量。这些创新不仅改善了临床决策,还为脊柱治疗中的数字孪生技术铺平了道路,其中模拟会根据真实的患者数据不断适应和调整治疗方案。 数字孪生建模与生物力学模拟 脊柱外科中的数字孪生建模利用MRI 或 CT 等成像技术创建患者脊柱的虚拟复制品。这些详细的三维模型映衬出患者独特的脊柱解剖结构,为手术规划提供了个性化方法。 人工智能,特别是深度学习算法,处理成像数据以快速准确地构建这些模型[40]。一旦构建完成,有限元分析(FEA)模拟脊柱在不同力作用下的行为,为术前规划和风险评估提供见解。脊柱疾病(如腰痛和脊柱侧凸)患病率的增加,凸显了对改进的生物力学评估和预测工具的迫切需求[16]。现代生活方式,包括长时间坐着、不良姿势和过度使用数字设备,都显著导致脊柱退变。在临床环境中,传统的CT 和 MRI 等成像技术有助于诊断结构异常,但仅限于静态评估,无法捕捉脊柱在运动过程中的动态行为。 这一差距对诊断和干预规划都构成了关键挑战,尤其是在考虑腰椎间盘突出症、小关节退变和脊柱侧凸进展等疾病的生物力学后果时[16]。数字孪生技术和人工智能的最新进展为实时监测和模拟脊柱生物力学提供了一个有前景的途径。数字孪生代表了一种虚拟的、自适应的脊柱模型,它集成了基于物理的模拟(例如有限元分析)和数据驱动的AI 模型。这使得能够在各种生理条件下连续跟踪脊柱行为。智能可穿戴设备(如惯性传感器和光纤系统)允许实时捕捉脊柱运动,这些数据可输入AI 算法以估算关键的生物力学变量,如小关节接触力和椎间盘内压力[35]。这种集成支持脊柱相关疾病(包括脊柱侧凸和慢性腰痛)的预测建模和个性化治疗计划[40]。 多项研究凸显了这项技术的强大功能。Liang等人 [78] 使用改进的U-Net(一种深度学习模型)自动进行腰椎建模。他们的方法达到了97.8% 的 Dice 相似系数,并在约10 分钟内生成了个性化的FEA 模型。这些模型帮助外科医生预测结果,例如植入物放置后的负荷分布,从而提高了手术精确度。进一步推进数字孪生技术,Ahmadi等人 [4] 将有限元分析与物理信息神经网络(PINN)相结合,对腰椎进行建模。使用CT 和 MRI 扫描,他们的方法自动化了椎骨和椎间盘的分割和网格划分,同时预测材料属性(如杨氏模量和泊松比),准确率达到94.30%。这种方法减少了人工操作,增强了患者特定模型的生物力学保真度,为术前规划和风险评估提供了一个强大的工具。 Ahmadian 等人[5] 开发了ReconGAN,这是一个基于3D 深度卷积生成对抗网络(DCGAN)的工具。仅用来自单个尸体椎骨的5 个长方体样本进行训练,ReconGAN合成了骨小梁结构,平均误差小于2%,并通过两点相关函数验证。他们的FEA 模拟显示,溶骨性病变的负荷减少了28%,成骨性病变的负荷减少了13%,为了解椎体强度提供了宝贵数据。Tajdari等人 [137]为青少年特发性脊柱侧凸创建了一个患者特定的有限元模型,结合AI 预测脊柱弯曲进展。这种方法使外科医生能够预见曲度严重程度并定制治疗方案,从而支持早期干预。 专注于椎间盘(IVD),Muñoz-Moya等人 [40] 从 MRI 扫描中创建了169 个腰椎 IVD 模型。经过离体验证,这些模型实现了超过92% 的形状相似性,为手术或康复期间椎间盘力学的精确模拟铺平了道路。Jecklin等人 [63] 采用了不同的方法,使用域适应技术从真实的透视图像重建3D 腰椎模型。他们的技术获得了84% 的 F1 分数,证明能够可靠地识别脊柱特征。该方法支持实时模型创建,可能有助于术中的FEA 模拟。 近期研究推动了AI-FEA 在脊柱外科中的整合。Lomax等人 [59] 强调了数字孪生技术在促进个性化术前和术后策略方面日益增长的作用。Singh等人 [16] 和 Luan & Morgan [34] 致力于改进患者特定建模,而Zheng 等人 [136]则专注于提高生理准确性,均保持了原始解剖和临床数据的高保真度。尽管取得了这些进展,但在将这些模型转化为常规临床实践方面仍存在若干挑战。例如,Garavelli等人 [35] 使用数字图像相关技术验证了患者特定的腰椎FEA 模型,显示出与实验的强一致性。然而,该研究强调了全面模型验证和不确定性量化的必要性,以确保临床可靠性。 同样,Molinari等人 [39] 研究了椎弓根螺钉角度的生物力学含义,确定尾内侧轨迹最安全。尽管如此,他们的发现受到骨折建模假设和缺乏定量验证的限制,强调了在数字孪生技术被广泛采用于临床脊柱外科之前进行严格测试的重要性。虽然取得了显著进展,但使数字孪生系统具备临床可行性仍面临挑战。许多现有的脊柱建模工作要么是静态的,要么过度依赖专用设备(如虚拟现实运动传感器),使其在日常实践中难以普及。此外,当前的模型通常缺乏足够的临床验证或在不同患者群体中的通用性[16]。为了推动该领域的发展,未来的研究应侧重于创建稳健、经过验证的数字孪生框架,这些框架能够使用标准临床数据和可穿戴传感器实时运行。这些系统可以通过实现早期诊断、预测疾病进展以及指导针对性的、患者特异性的治疗来彻底改变脊柱治疗[59]。 AI 增强的手术规划 人工智能与有限元分析相结合,通过在术前规划中提供精准的生物力学洞察,增强稳定性并降低风险,从而改变脊柱外科。例如,Ma等人 [35] 开发了一个基于机器学习的FEA 系统,用于优化骨质疏松脊柱中的椎弓根螺钉轨迹。与传统方法相比,该方法使拔出力提高了2.0-4.6 倍,展示了 AI分析复杂脊柱几何形状和负荷条件的能力。在临床上,这转化为降低的固定失败风险、更少的翻修手术和改善的长期患者结局,如增强的脊柱稳定性和减少的术后疼痛。Zhou和Willing [137] 利用人工神经网络和多目标优化来改进双凹面活动轴承人工椎间盘设计。通过FEA 平衡活动范围、小关节负荷和接触力学,他们的方法旨在改善TDA 结果,展示了AI 在术前植入物优化中的作用。 类似地,Phellan Aro 等人 [92] 使用随机森林预测术后脊柱对线,RMSE为 3.75±0.56 毫米,使外科医生能够在手术前预见并解决潜在的对线问题。该模型使用随机森林(一种具有优化超参数的决策树集成)来捕捉术前变量与术后结果之间的非线性关系。高预测精度允许进行定制干预,从而改善患者活动能力并减少邻近节段退变等并发症。其他研究进一步展示了AI-FEA 在术前规划中的能力。Jimenez等人 [16] 模拟了创伤性脊髓损伤中的脊髓压迫,曲线下面积(AUC)达到0.79-0.82。Tajdari等人 [136]预测青少年特发性脊柱侧凸曲率,误差范围为0.60% 至 10.43%。Peng 等人 [78] 开发了一个基于神经网络的工具,用于优化脊柱侧凸手术中的近端交界角,以83.3% 的准确率预测术后近端交界性后凸风险。这种个性化方法帮助外科医生定制手术计划以尽量减少并发症。 图 4 详细阐述了人工智能在改善脊柱手术结果方面的创新应用。 此外,Burns等人 [8] 开发了一个自动化系统,用于在CT 图像上检测椎体压缩性骨折,进一步增强了AI 在术前风险识别中的作用。该系统实现了95.7% 的灵敏度和每患者0.29 的假阳性率,可识别高风险患者,使外科医生能够调整计划(如植入物选择或螺钉放置)以尽量减少术中并发症并改善结果。Jamaludin等人 [35] 开发了SpineNet,一个基于CNN 的框架,可自动对腰椎MRI 进行分级并定位椎间盘退变和椎管狭窄等病理。SpineNet在多个级别上实现了接近人类的表现,通过提供快速、准确的评估来增强术前诊断,可能减少治疗计划的延误。Suzuki等人 [39] 使用 CNN 从普通 X 光片中检测腰椎管狭窄症,在外部验证中达到了0.90 的 AUC 和 82% 的准确率。该工具有助于早期诊断,可能减少治疗延误。为了解决FEA 的计算负担,Atad等人 [8] 引入了一个神经网络代理结合投影梯度下降法,用于校准L4-L5 椎间盘的有限元模型。他们的方法在合成数据上实现了0.06 的平均绝对误差,并将校准时间缩短到3 秒以下,而传统方法则要长得多。这种快速、准确的校准可以使实时生物力学模拟成为可能,增强患者特异性手术规划的可行性。此外,将神经网络代理纳入深度学习框架,例如[8] 中提出的框架,可以显著提高脊柱手术规划的准确性。 新的研究补充了这些发现。Pedersen等人 [16] 引入了PROPOSE,一个机器学习工具,用于预测腰椎管狭窄症手术后的结果(如行走距离改善,AUC 0.88)和疼痛缓解,有助于共同决策。Schonfeld等人 [59] 使用卷积神经网络和大型语言模型预测成人脊柱畸形手术后的并发症,肺部并发症的F1 分数为0.545。Pellise等人 [89] 利用放射组学和机器学习预测机械并发症,其AUC-ROC 为 0.75,优于传统放射学测量的0.71。此外,Karhade等人 [39] 和Alassaf 等人 [8] 解决了植入物失败风险,而Varghese 等人 [71] 增强了时间依赖建模,所有这些都支持了AI-FEA 在手术规划中的进展。与依赖外科医生经验且通常精度较低的传统手动规划相比,AI-FEA工具提供了显著的飞跃。例如,Liang等人 [78] 在其 AI 驱动的分割模型中报告了97.8% 的 Dice 相似系数,远超通常徘徊在80-85% 的传统方法。尽管取得了这些进展,但仍存在局限性。许多这些模型是在相对较小或同质的数据集上验证的,这引发了对其在不同患者群体中通用性的担忧。未来的研究可以侧重于扩展这些数据集并整合额外的变量,如遗传或生物标志物数据,以进一步个性化手术计划。 表 3 总结了在脊柱手术的术前、术中和术后阶段结合AI-FEA 的关键研究。它强调了应用于螺钉放置、脊柱建模和风险预测等任务的多种AI 方法(如U-Net、PINN、AR)。报告的结果包括高精度、缩短的处理时间和提高的手术精确度。这些进展展示了AI-FEA 整合如何以更高的准确性和效率重塑手术规划。 表 3 关于脊柱外科中AI-FEA 的关键研究总结 与智能可穿戴设备和物联网在脊柱康复中的整合 智能可穿戴设备和物联网技术的整合显著改变了脊柱康复和恢复的格局。脊柱外科医生传统上依赖经过验证的工具,如患者报告的疼痛水平、功能残疾评分、影像学发现、抑郁指数和药物使用情况来评估治疗结果。然而,包括功能评估等客观指标在内的残疾和功能结果测量的加入增加了新的临床洞察层面,正逐渐成为常规护理的一部分。随着可穿戴设备的兴起,特别是在COVID-19 大流行之后,对用户友好且易于使用的技术的需求日益增长,这些技术可以提供有关患者脊柱健康的实时、可量化数据。这些可穿戴工具——从智能手表到运动传感器和基于手机的应用程序——使临床医生能够在真实世界环境中,在临床环境之外跟踪身体功能,如躯干运动、步行速度和姿势。通过将可穿戴设备与远程医疗系统集成,医疗保健提供者可以提供更个性化和持续的护理,尤其是在术后恢复期间。 术后护理与手术本身一样重要,可穿戴技术和物联网设备的最新进展已经改变了监测和康复阶段。可穿戴传感器可以连续监测脊柱姿势、检测不对称性并跟踪恢复过程中的进展[156]。这些设备生成实时的生物力学和生理数据,可以输入AI 算法以动态调整物理治疗方案。结合AI,可穿戴设备还可以通过监测局部温度、肿胀或运动模式等迹象来预测感染、血栓或植入物整合不良等并发症。与基于智能手机的仪表板的集成允许患者和临床医生保持持续的沟通和反馈回路,提高依从性和满意度[63]。 图 6 人工智能、物联网和增强现实技术在脊柱恢复和康复中的整合 关键创新包括用于姿势监测的智能传感器矫形器、用于连续患者跟踪的物联网实时平台,以及用于增强患者教育和参与的AR 工具 [12, 147]。这些技术旨在改善结果并个性化护理,但仍存在若干挑战。 其中,AR、LLM 和数字健康生态系统的整合显示出在提供可及、高效和智能的脊柱康复解决方案方面的巨大潜力。 可穿戴技术和人工智能的持续进步为脊柱护理中的预测分析开辟了新的可能性。这些工具可以通过捕获日常活动中的纵向生物力学数据(传统上难以收集的数据)来帮助制定个性化治疗计划[21, 99]。尽管存在一些局限性,例如目前对实验室环境的依赖和校准挑战,但可穿戴传感器正逐渐成为脊柱健康监测的重要组成部分。未来的方向指向一个更全面、由AI 驱动的生态系统,该系统不仅远程监测患者,还基于实时功能反馈支持决策、依从性和量身定制的康复方案。 教育影响:基于AI 的手术模拟 脊柱手术的学习曲线仍然很陡峭,尤其是对于复杂手术,如畸形矫正或多节段融合。传统的培训方法通常依赖于尸体实验室、有监督的实践和耗时的观察。然而,AI驱动的模拟器和虚拟现实(VR)/增强现实(AR)平台正在重塑外科教育[7]。这些平台使用真实的患者数据来模拟各种手术场景。AI实时跟踪学员的表现,就施力、工具轨迹、解剖定位和手术步骤提供反馈。随着AI 模型接触到更多的手术案例,它们在模拟真实世界的结果和错误方面变得更加准确[16]。 此外,VR/AR模拟允许安全地重复高风险操作。住院医师和进修医师可以在不危及患者安全的情况下练习多种手术变体。当与触觉反馈和图像引导跟踪系统结合时,这些模拟器提供了一个近乎真实的训练环境。将AI 模拟整合到标准化的住院医师课程中,也有助于平衡各机构的培训质量。在发展中地区,便携且低成本的VR 训练器可以弥补无法接触真实手术或高端设备的不足,支持更公平的医疗workforce。 通过 AI 文献挖掘加速脊柱研究 人工智能,特别是自然语言处理(NLP)和大型语言模型(LLM)的整合,通过能够自动解析非结构化临床数据,显著加速了脊柱研究的步伐。传统上,脊柱手术中的放射学报告、手术记录和知情同意书需要人工审阅,这使得数据提取劳动密集且容易不一致[21, 63]。然而,在大量临床文本语料库上训练的NLP 工具(如BERT、LLaMA-7B和微调的 GPT模型)的出现彻底改变了这一过程。这些工具能够准确识别关键的手术事件(如意外硬膜切开、伤口引流使用、闭合类型),根据疼痛位置和急性程度对肌肉骨骼疼痛特征进行分类,并根据知情同意书对脊柱手术进行分类,其性能指标通常超过90% 的准确率、灵敏度和预测值[59]。 脊柱研究的激增创造了一个庞大而fragmented 的知识体系。手动审阅数百篇关于脊柱植入物、手术技术或生物力学的论文可能令人不知所措。 AI 工具现在通过自动化文献挖掘、趋势分析甚至假设生成来促进科学发现。自然语言处理算法用于从数千篇研究文章中提取信息,识别技术、结果和患者群体之间的联系。例如,基于文献和患者数据的横断面分析,AI可以快速检测到65 岁以上患有骨质疏松症且接受后路腰椎融合术的患者更容易发生螺钉松动[16]。 图 7 多模态人工智能系统用于椎间盘突出诊断和决策 该系统使用基于transformer 的架构将医学影像与临床语言相结合,为医疗保健提供者和患者生成针对性的建议。工作流程从输入脊柱MRI 图像开始,随后是关于检测到的椎间盘突出的自然语言提示。问题(针对脊柱专家和患者)使用集成了视觉和临床语言的transformer 架构进行处理。输出包括AI 生成的关于临床行动的建议,如评估患者症状、评估严重程度以及决定保守或手术治疗方案。该流程突出了AI 从影像和文本中挖掘和综合知识以加速脊柱研究和改善结果的潜力。 生成模型还可以总结整个研究领域,生成科学合作网络的可视化图谱,并根据相关性和新颖性推荐文章。这加速了跨学科研究,使得AI、FEA、材料科学和临床学科之间能够更快地创新。在研究资助计划或系统评价中,此类AI 工具通过根据技术内容和统计强度对论文进行分类,减少了时间并提高了纳入/排除标准的客观性[8]。这些工具还可以检测发表偏倚或冗余试验,指导研究人员关注具有未满足临床需求的高影响力主题[3]。 表 5 总结了各种应用(包括诊断、治疗计划、风险评估和指南解读)中的方法、目标和结果。 AI 驱动的文献挖掘还提供了一种可扩展且保护隐私的方法,用于利用以前因非结构化性质而未得到充分利用的历史数据。研究表明,NLP算法可以从脊柱影像报告中提取详细的放射学结果,从而无需昂贵的人工注释即可实现对深度神经网络的弱监督学习[35, 95]。这种方法提高了训练效率,并支持开发用于手术结果、并发症风险和三联需求的预测模型。此外,从现有临床文档生成的AI 结构化注释有助于识别研究队列,为放射学质量评估提供信息,并支持流行病学研究,从而有助于更全面和循证的脊柱护理[16]。 尽管 AI 在脊柱文献挖掘中具有变革潜力,但某些局限性仍然存在。通用LLM 在未针对医学领域进行微调时可能会产生幻觉或提供过于笼统的响应,引发对临床可靠性的担忧。此外,文档风格的差异和手术记录缺乏标准化对模型的泛化能力构成了挑战。尽管如此,在指令调优模型、为保护患者隐私而使用本地托管AI 系统以及遵守机器学习报告指南(如TRIPOD、JMIR)方面的持续进展正在积极解决这些差距。因此,AI增强的文献挖掘不仅加速了回顾性脊柱研究,而且为未来临床应用中的预测分析和决策支持系统奠定了基础。 用于手术规划和器械优化的AI 驱动脊柱建模的整合 人工智能在脊柱外科中的整合正在重新定义临床医生如何进行手术规划和植入物开发。传统上,植入物设计依赖于静态的通用模型,这些模型无法完全模拟脊柱在动态生理条件下的复杂生物力学行为。随着AI 驱动模拟的采用,现在可以开发适应性强且患者特异性的脊柱模型,这些模型包含解剖变异、负荷条件和材料属性。这些模型不仅更准确,而且可以预测潜在的失效点和应力集中,最终实现更安全、更有效的手术干预。机器学习算法,特别是那些在包括医学影像、患者人口统计学和术后结果在内的大型数据集上训练的算法,已经实现了支持手术室中实时决策的预测建模。AI通过调整手术方法和器械配置以适应每位患者的独特特征,增强了个性化护理。包括实时成像和监测在内的术中数据可以整合到AI 模型中,为外科医生提供动态指导。这种个性化和自适应支持提高了手术操作的精准度并改善了患者结局,特别是在涉及脊柱畸形或退行性疾病的复杂手术中。 图 8 AI 驱动的脊柱护理工作流程,整合了基于成像的模拟、个性化器械设计和手术应用。患者特异性脊柱模型指导手术规划、告知器械定制并支持术中的实时决策,形成一个用于优化结果的闭环系统。 表 6 提供了当代研究的广泛概述,这些研究探索了AI 驱动方法在脊柱建模、诊断和手术优化中的整合。一些综述和原始研究(例如[21, 63, 77])讨论了机器学习、成像分析和基因组学在转变个性化脊柱护理中的作用。新兴框架,如算法-硬件-伦理 [54] 和用于癌症诊断的联邦学习[21],为稳健且安全的AI 部署提供了新途径。 此外,正在开发AI 驱动的数字孪生体,以虚拟复制患者的脊柱,从而能够在术前测试不同的手术场景。这些虚拟模拟允许外科医生在进入手术室之前评估植入物性能并优化器械放置。先进的AI 模型还通过预测植入物松动或邻近节段疾病等并发症来协助术后监测。AI的影响在下一代植入物的开发中尤为显著,这些植入物能够动态适应患者的生活方式和负荷条件。镁基合金等材料与机器学习驱动的优化相结合,使研究人员能够模拟植入物在各种活动(如行走或弯曲)下的行为。这些洞察在制造之前指导材料选择和结构设计,促进更耐用、生物相容且功能适应性更强的植入物。随着AI 的不断发展,它整合到从诊断到植入物设计和术中导航的整个手术流程中,将在彻底改变脊柱护理和实现真正个性化、以结果为导向的治疗路径方面发挥关键作用。 标准化和互操作性 为了使AI-FEA 模型在临床中得到整合,标准化是必不可少的。目前,大多数模型是在特定机构的数据上使用专有软件流程构建的。这限制了不同医院和研究中心之间的可重复性和互操作性。正在努力创建用于脊柱分割、材料映射和网格生成的通用协议。开源库和共享数据存储库,如SpineWeb、TotalSegmentator和 MICCAI挑战数据集,正在使标准化基准更容易获得[4]。这些资源能够公平比较模型性能并促进透明度。 此外,兼容DICOM 的 FEA 流程和流行医疗平台(如3D Slicer、OsiriX)的 AI 插件使临床医生能够直接在治疗计划中使用模拟结果。将AI-FEA 工具与医院信息系统和EHR 集成,还能提高工作流程效率并支持床旁决策。然而,互操作性需要在文件格式、标签约定和数据预处理步骤上达成共识。监管机构、软件供应商和医学协会之间的合作对于制定平衡准确性、计算需求和可用性的标准是必要的(图9)。 这个多机构流程强调了协调一致的成像协议和统一标签的迫切需求,确保AI 模型在不同的临床环境中表现一致[71, 119]。通过 FEA 在各种负荷条件(如屈曲、伸展、侧弯和轴向旋转)下进行的生物力学模拟,进一步丰富了AI 导出的分类。为了保持一致性,这些模拟必须应用标准化的边界条件、材料属性和负荷参数。由此产生的定量输出,如椎间节段的应力分布,为临床决策提供了宝贵的见解,但前提是结果既要可解释又要标准化[16, 95]。 要使AI-FEA 系统成为可互操作的临床工具,从数据标记和CNN 训练到 FEA 建模和输出解释的每个组成部分都必须符合通用框架、网格标准、命名约定和解剖标志。随着这些技术的发展,构建一个共享的工具、数据库和协议生态系统对于将脊柱诊断转变为可扩展的、患者特异性的解决方案至关重要[12]。 图 9 用于可互操作脊柱诊断的标准化AI-FEA 工作流程 随着 AI 的不断发展,半自主或完全自主脊柱手术的前景变得更加现实。机器人平台,如Mazor X 和 ROSA Spine,已经在椎弓根螺钉置入中提供AI 引导的辅助,其准确性超过了传统方法。未来的系统可能会结合实时成像、AI驱动的解剖识别和基于FEA 的力反馈预测,使机器人系统能够在最少的人工干预下执行减压、椎间盘切除或融合等任务。外科医生将从手动操作者转变为监督者,验证AI 的决策,并仅在出现意外情况时进行干预[12]。 自主系统还可以提高偏远地区或战场环境中的安全性,在这些环境中,获得脊柱外科专家服务的机会有限。结合5G 赋能的远程手术平台,AI驱动的机器人系统可以跨越地理边界提供高质量的医疗服务。尽管如此,仍然存在重大的法律、伦理和技术障碍。确保实时错误检测、实施安全超控和建立责任框架对于广泛采用至关重要。 手术规划和导航是自主脊柱手术系统的基本要素。这一阶段从术前阶段开始,利用CT 或 MRI 等医学成像技术构建患者特定的解剖模型。然后通过计算机辅助模拟工具处理这些模型,以制定针对患者解剖结构的精确手术策略。这种模拟不仅有助于确定最佳轨迹和进针点,而且还能最大限度地降低术中风险。AI-FEA增强了手术执行的精度。Ao等人 [12] 开发了SafeRPlan,一种用于椎弓根螺钉置入的深度强化学习工具,与传统方法相比,安全性提高了5% 以上。这降低了螺钉错位的风险,Riewruja等人 [99] 发现传统病例中螺钉错位发生率为5-10%,他们的荟萃分析显示机器人辅助系统在准确性上优于传统、导航和增强现实方法。Khalsa等人 [21] 回顾了脊柱机器人的发展历程,指出当前系统仅限于螺钉置入引导,但强调了通过与先进规划软件和导航集成,未来有可能将其效用扩展到复杂手术中。Wang等人 [124]回顾了脊柱手术中的机器人导航,追溯了其自2004 年以来的发展并评估了当前技术。虽然主要用于椎弓根螺钉置入,但他们指出快速进展有望带来更广泛的应用,提高手术精度和效率。Tariciotti等人 [119]系统回顾了 AI在神经外科工作流程中的应用,重点强调了术中手术辅助。他们强调AI 和 ML,特别是神经网络和基于树的模型,如何增强决策、减少人为错误并提高包括脊柱外科在内的各个亚专科的手术精度。 图 10 自主脊柱手术系统的完整工作流程,涵盖三个主要阶段: 此外,Youssef等人 [92]、Zhang 等人 [39]、Bui 等人 [21]、Siemionow等人 [63]、Burstrom等人 [16] 和 Von Atzigen 等人 [148]的研究通过 AR辅助的椎弓根螺钉置入、空间配准方法、AR/VR应用以及棒弯曲导航改进,推进了手术规划和导航。Youssef等人 [92] 报告 AR 辅助螺钉置入的临床准确度为93.1%,而 Zhang等人 [39] 实现了 AR 导航的表面配准误差仅为0.501 毫米。Bui 等人 [21] 强调了AR/VR 在手术演练和执行中的实用性,Siemionow等人 [63]、Burstrom等人 [16] 和 Von Atzigen 等人 [148]为棒弯曲等任务的导航增强做出了贡献,保留了Zhang 等人 [95] 的关键指标,如92.8% 的 3D Dice 指数。 这些进展共同减少了术中错误、简化了工作流程并提高了患者安全性。此外,将AI-FEA 与机器人手术系统和增强现实等新兴技术相结合,有望进一步提高精度和效率。 表 7 总结了各种脊柱和颅脑手术中手术规划、导航和评估技术的最新进展。 例如,将AI-FEA 与机器人技术相结合可以自动化螺钉插入等任务,而基于Youssef 等人 [92] 工作的 AR 叠加可以提供AI 生成模型的实时3D 可视化。然而,挑战依然存在,包括高计算需求以及需要更广泛的验证,正如Zhang 等人 [95] 的对照研究所指出的。此外,无缝集成到现有手术室系统需要解决资源限制并确保与当前工作流程的兼容性。 表 7 脊柱及相关手术中AI 驱动的手术规划、导航系统和结果评估的关键研究总结 表 8 概述了人工智能驱动的有限元分析与增强现实和机器人技术在整个手术工作流程中的协同整合。在术前阶段,AI-FEA有助于模拟患者特定的脊柱力学,而AR 和机器人技术则增强可视化和螺钉路径规划。在术中阶段,实时数据完善FEA 预测,机器人系统确保精确的器械控制,AR辅助手术导航。在术后阶段,FEA模型和 AI 监测植入物整合和患者结果,机器人工具支持康复。这种协同作用实现了个性化、数据驱动且减少错误的脊柱手术。 在术中阶段,手术导航系统通过将器械和解剖结构的实时跟踪与预先规划的手术策略相结合而发挥核心作用。通过使用术中配准和数据融合持续更新手术区域,外科医生在手术过程中以高精度获得引导。配备传感器并由计算机视觉引导的机器人手臂在人工监督或半自主控制下执行这些计划,显著提高了准确性和可重复性。机器人平台是自主系统的基石,为手术任务提供了无与伦比的精度。这些系统增强了术中导航和执行,最大限度地减少了人为错误,并提高了椎弓根螺钉置入等手术的准确性。 表 8 新兴技术:AI-FEA与 AR/机器人的协同作用 表9脊柱研究及临床应用中影像、计算和患者报告数据模式概览 术后评估与预测建模 AI 驱动的有限元分析对于增强术后护理至关重要,可提供关于生物力学风险、并发症和功能恢复的个性化预测。通过将AI 与 FEA 模拟和临床数据相结合,这些工具使临床医生能够制定量身定制的康复策略并主动管理术后护理。 例如,Berg 等人 [12] 开发了机器学习模型来预测腰椎间盘突出术后患者的残疾和疼痛。他们的模型对Oswestry 残疾指数的 C 统计量达到0.82,反映了强大的预测准确性。该模型在多个地区得到验证,可提供个性化的预后洞察,从而实现量身定制的康复计划和改进的术后患者咨询。Kalagara等人 [12] 开发了机器学习模型来预测腰椎椎板切除术后再入院,使用出院前变量实现了超过79% 的准确率。该工具通过识别高风险患者,支持术后护理,能够进行有针对性的干预以降低再入院率。AI还帮助预测AIS 的术后结果。Goldman等人 [12] 强调的模型预测曲线进展的平均准确率为85.4%,为临床医生监测和规划后续干预提供了宝贵的见解。尽管取得了这些进展,但仍存在局限性。 图 11 展示了基于AI-FEA 的术后风险预测工作流程。通过整合成像数据和临床记录,AI增强的有限元模拟估算应力、应变和位移等生物力学参数。然后,这些生物力学特征被输入机器学习模型,以预测关键的术后结果,包括骨折概率、压力性损伤风险以及由Oswestry 残疾指数测量的功能恢复。这种方法能够早期识别并发症并支持个性化康复计划。 图 11 基于AI-FEA 的术后风险预测工作流程 此外,实时FEA 模拟的计算需求对广泛临床应用构成了障碍。未来的研究应侧重于在不同患者群体中进行前瞻性验证,并探索与可穿戴传感器或AI 引导的康复应用程序等技术的整合,以增强实时监测和患者参与度。 患者影像和临床数据用于模拟生物力学应力并训练预测模型,为脊柱手术后骨折风险、压疮可能性和功能恢复等关键结果提供估计。 挑战与未来方向 AI-FEA 在脊柱外科中的采用面临着显著的实施障碍,主要与计算和财务需求有关。这些模型的高计算复杂性需要大量的处理能力,这可能并非所有临床环境都具备。这直接导致了实施的财务负担,因为采购和维护先进的术中成像、导航系统和专用硬件需要大量资金。虽然这些技术可以通过减少翻修手术带来长期节省,但高昂的前期成本对许多机构构成了主要障碍。 第二个主要障碍涉及模型验证和临床整合。许多当前的AI 模型是在有限或同质的数据集上训练的,这引发了对其在不同患者群体中通用性的担忧。 因此,需要投资于大规模、多机构的数据收集和验证研究。此外,外科医生和工作人员面临陡峭的学习曲线,通常需要20-30 例病例才能达到熟练程度。将AI-FEA 的复杂输出整合到现有手术工作流程中具有挑战性,并且可能最初会延长手术时间,这凸显了对全面且可访问的培训计划的需求。除了后勤和财务障碍外,仍然存在重大的伦理和监管挑战。确保患者数据隐私至关重要,并且正在探索联邦学习等分散方法,以便在不共享敏感患者数据的情况下训练模型。此外,为AI-FEA 工具的临床批准建立明确的监管途径和标准化协议对于其安全广泛采用至关重要。 克服这些障碍的未来方向必须侧重于实用的、多管齐下的策略。这包括通过创新的购买或租赁模式提高成本效益,投资于基于模拟的全面培训以减少学习曲线,并促进进一步研究以增强这些技术的临床和经济证据。将AI-FEA 与机器人和增强现实等赋能平台整合,为创建更强大、更直观的系统提供了有前景的途径。最终,克服这些多方面的障碍将取决于临床医生、工程师和政策制定者之间的合作努力,以在促进创新的同时确保患者安全和公平获得这些变革性技术。 结论 人工智能与有限元分析的整合代表了脊柱外科的一个重大范式转变,实现了个性化、可预测和数据驱动的干预。AI增强的 FEA 允许快速、高保真度的生物力学模拟,支持手术规划、术中导航和术后风险评估。这些模型使临床医生能够根据个体解剖结构、生理反应和预测的并发症定制治疗策略,最终改善结果并降低手术风险。从优化的椎弓根螺钉置入到先进的椎间盘建模,AI-FEA的临床影响显而易见。PINN等新兴技术用于材料预测和快速代理模型校准,预示着AI-FEA 将提供实时、患者特异性模拟的未来。许多现有模型依赖于有限或同质的数据集,这可能限制其对不同患者群体的通用性。实时模拟仍然需要高性能计算资源,这在所有临床环境中都不易获得。此外,监管不确定性、缺乏标准化工作流程以及对数据隐私和算法透明度的伦理担忧继续对广泛临床采用构成障碍。为了克服这些挑战,未来的努力必须侧重于前瞻性临床验证、更广泛的多机构数据整合以及开发可解释、透明的AI 系统。纳入可穿戴传感器、智能植入物和电子健康记录连接将进一步增强实时反馈和自适应决策。最终,实现AI-FEA 在脊柱外科中的全部潜力需要临床医生、生物医学工程师、计算机科学家和政策制定者之间的紧密合作。如果成功实施,AI-FEA可能成为下一代智能脊柱护理系统的基础技术,大规模提高安全性、效率和患者结果。