AI解码脑疾病,开启精准诊疗新可能
(本文阅读时间:10分钟)
随着全球人口老龄化不断加深,阿尔茨海默病、帕金森病等神经退行性疾病的发病率持续攀升。这类疾病起病隐匿、进展缓慢,且发病机制尚未明确,长期以来缺乏有效的早期诊断手段、高效的治疗药物以及个性化的病程管理方案,已成为全球医疗卫生领域亟待攻克的重大挑战。
人工智能技术的快速发展,为复杂神经疾病的研究与诊疗开辟了全新路径。凭借对多模态异构数据的处理能力、对潜在关联规律的挖掘能力,以及更强的预测与推理能力,AI有望从基础研究到临床应用,重塑神经疾病诊疗的全流程体系。
微软亚洲研究院(上海)长期深耕人工智能与脑科学交叉领域,围绕神经疾病诊疗中的核心难题持续探索并取得了突破。近年来,团队针对阿尔茨海默病多模态数据融合难题,构建了统一的多模态诊断框架;在脑靶向药物递送领域实现了对血脑屏障关键瓶颈的研究范式突破,探索建立人机协作的闭环研发体系;同时,在帕金森病病程预测中提出了AdaMedGraph图神经网络方法,首次实现了个性化的病程建模和预测。
从诊断模型到药物研发,再到病程管理,这些研究成果为长期缺乏有效解决方案的神经退行性疾病提供了新的思路,也推动脑部疾病诊疗向更精准、高效和个性化的方向持续演进。
相关论文已整理于文末,欢迎点击相关链接,了解更多技术详情。
在神经退行性疾病研究中,科研人员通常面临多重难题:如何在症状尚未显现时实现早期识别;如何让药物真正跨越血脑屏障,进入大脑发挥作用;以及如何理解不同患者之间差异显著的病程演化?这些问题持续制约着神经疾病的基础研究与临床实践的进展。对此,微软亚洲研究院(上海)团队展开了一系列探索。
1. 从“单一视角”到“多模态融合”:推动阿尔茨海默病早期诊断迈出关键一步
阿尔茨海默病(AD)的临床诊断通常需要综合多种检查手段,如认知量表评估、磁共振成像(MRI)、血液生物标志物检测及基因测序等。尽管针对单一模态的AI模型已展现出强大的性能,但医生仍需手动整合多个独立模型的输出结果进行综合判断,增加了临床医生的决策成本。
然而,将多个高性能单模态模型整合为统一的框架在机器学习上面临着巨大的挑战。这需要对齐不同模型的特征空间、融合其输出结果,才能充分利用互补信息,让基础模型实现有意义的交互。研究员们发现,由于每个基础模型的预训练目标都是捕捉独特的单模态特征,其表征具有固有的异质性与结构化特点。若简单对齐或融合这些特征空间,可能无法有效利用不同模态间的互补性,甚至导致性能下降。
如何在实现基础模型的充分交互与保留其预训练特征空间完整性之间取得平衡?微软亚洲研究院(上海)联合同济大学提出了一种基于模态锚定基础模型交互的统一多模态阿尔茨海默病诊断框架。该方法以一种模态作为锚点,保留其原有特征空间结构,同时通过全新设计的模态感知查询转换器Q-former,将其他辅助模态的特征精准映射至锚点空间,从而实现跨模态信息的有效对齐与融合。
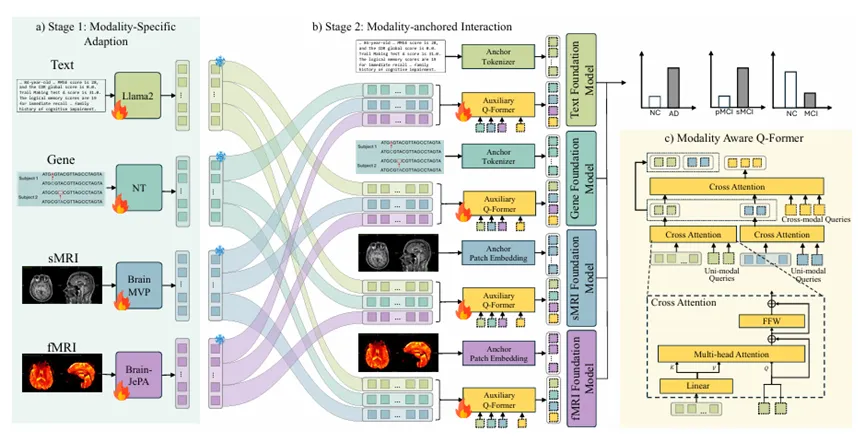
图1:多模态阿尔茨海默病诊断框架流程
这一框架首次整合了阿尔茨海默病相关的三类核心数据:基因数据、神经影像数据和临床数据。在更全面的模态覆盖基础上,结合对基础模型的适配策略,模型能够更深入地理解疾病的病理机制,提升诊断精度。同时,该方法还展现出强大的泛化能力,可扩展应用于帕金森病等其他神经退行性疾病。
Joint Adaptation of Uni-modal Foundation Models for Multi-modal Alzheimer’s Disease Diagnosis (已被 ICLR 2026 接收)
论文链接:https://openreview.net/forum?id=gPTjQxC74G
2. 让药物真正进入大脑:“人机协作”重构脑靶向药物研发路径
如果说早期诊断是疾病研究的第一道关口,那么如何让药物有效进入大脑,则是另一道公认难题。人体的血脑屏障能有效保护大脑免受有害物质侵入,但同时也导致98%以上的药物分子无法穿透这一屏障抵达病灶。
传统的药物筛选方法主要依赖反复试错,通过大量实验逐步筛选具有潜在穿透能力的候选分子。这种方式不仅周期漫长、成本高昂,而且成功率有限,往往需要多年时间才能验证少数可行方案。
为打破这一瓶颈,微软亚洲研究院(上海)联合复旦大学药学院,构建了一套实验室闭环(lab-in-the-loop)机器学习框架,将人工智能模型与实验验证紧密结合,形成持续迭代的闭环系统。
研究员们首先从跨越半个世纪的9500篇相关文献中提取出17600个特征,然后训练出能够精准预测纳米药物递送系统穿透效率的专用模型。模型完成初步筛选后,AI生成的候选方案会进入实验环节进行验证;实验结果再反馈至模型,用于持续优化算法。通过“预测-验证-再学习”的循环机制,整个研究过程从传统试错模式,转向更高效、更精准的数据驱动预测模式。
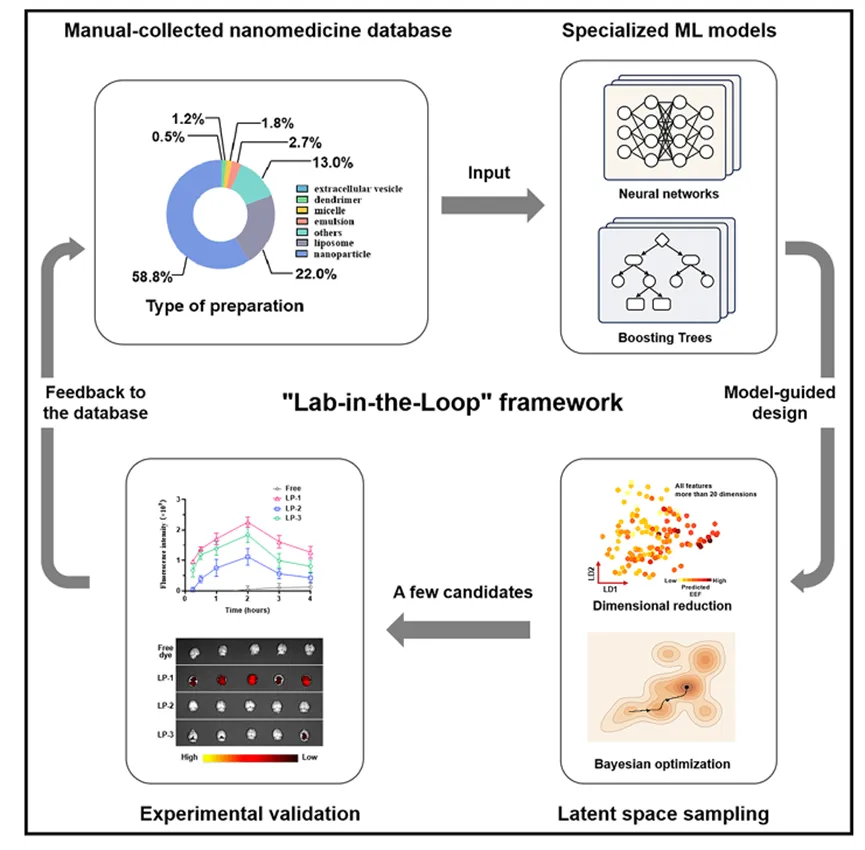
图2:实验室闭环框架
借助这一方法,研究员们识别出粒径(Particle Size)和表面电位(Zeta Potential)等多项影响脑靶向递送效率的关键参数。在实验验证中,由AI设计的递送系统在脑部的富集效率提升达十倍之多。这种“人机协作”模式不仅为脑靶向药物设计提供了新的路径,也有望在更多复杂药物研发任务中发挥价值,加速新药从实验室走向临床的进程。
Lab-in-the-loop machine learning for brain-targeting delivery system design (已发表在Cell Biomaterials期刊)
论文链接:https://www.sciencedirect.com/science/article/pii/S3050562325001217
3. 读懂每位患者的“疾病轨迹”:构建帕金森病个性化预测模型
当精准诊断与高效药物递送形成合力,神经疾病诊疗仍需要一套动态系统来监测治疗效果、提前预判病情走势。即便同一种疾病,在不同患者身上的进展轨迹也截然不同。以帕金森病为例,不同患者的症状进展速度、对药物的反应存在显著差异。而传统预测模型仅能实现群体层面的趋势判断,无法为个体提供精准的病程预判。
为更好地刻画个体差异,微软亚洲研究院(上海)与香港大学合作于2024年提出了AdaMedGraph图神经网络模型。其核心思路是将患者间的相似关系转化为图结构表示,借助相似患者的信息辅助个体预测。在这一网络中,每位患者不仅由自身数据描述,还能通过与其他患者的关联获得额外信息支持,使模型更全面地理解疾病的演变过程。
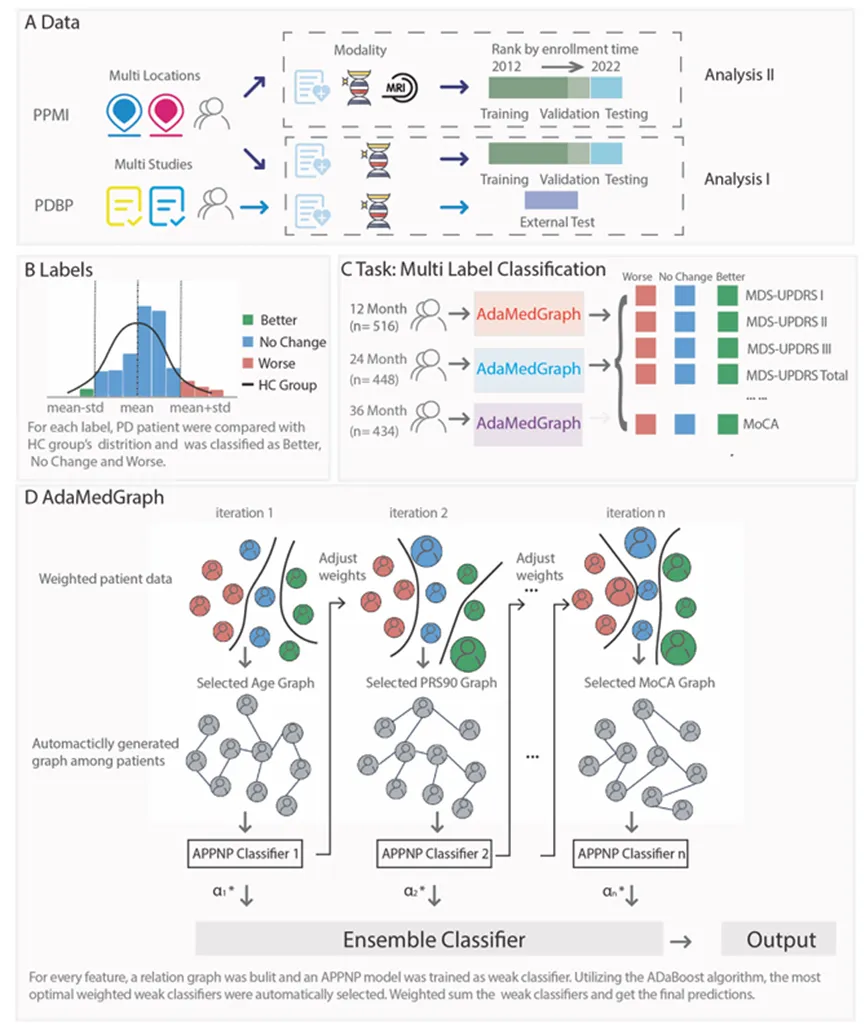
图3: AdaMedGraph示意图
实验结果显示,该模型能够对帕金森病患者在未来12、24和36个月内的多维病程进展进行预测。这意味着医生不仅能掌握患者当前状态,还能预判其未来的病程演变趋势,进而制定更科学、更个体化的治疗与管理方案。
Personalized progression modelling and prediction in Parkinson’s disease with a novel multi-modal graph approach (已发表在Nature 旗下npj Parkinson’s Disease期刊)
论文链接:https://www.nature.com/articles/s41531-024-00832-w
“从阿尔茨海默病的早期诊断、脑靶向药物的筛选,到帕金森病的病程管理,这些研究并非彼此孤立,而是在共同指向一个更完整的目标。”微软亚洲研究院首席研究员李东胜表示,“我们希望以全周期、全场景为出发点,推动AI深度融入神经疾病诊疗的全过程。”
这一判断,源于AI在神经疾病领域所展现出的巨大潜力。随着数据、算法与算力的协同演进,AI正逐步改变这一领域的研究范式。
一方面,借助数据规模效应(scaling law),模型不仅可以利用有限的患者数据,还能够融合海量健康人群与多类型疾病数据进行预训练,再通过有针对性的微调突破小样本临床数据的限制。另一方面,新一代AI算法正在超越传统统计分析框架,既可以挖掘复杂数据间的关联,也能够探索疾病与多组学数据之间的潜在因果机制,为理解神经疾病的深层机理提供新的工具。与此同时,高效算力的引入,使科研流程可以更快速的迭代,大幅提升了从发现到验证的整体效率。
在此基础上,微软亚洲研究院正逐步构建覆盖全流程的脑健康AI研究体系,贯穿机理理解、药物发现、早期诊断、个性化治疗,以及病程预测与康复训练等关键环节。例如,在机理研究中,研究员们通过帕金森病建模发现,不同基因型与表征的患者对左旋多巴的反应存在显著差异,为理解疾病机制提供了新的线索;在药物发现方面,除脑靶向递送研究外,研究员们此前还探索出潜在的药物组合策略,为拓展神经疾病治疗路径提供可能;在早期诊断方面,团队数年前便研发出语音分析模型,用于阿尔茨海默病无创筛查;在康复阶段,“忆我”(ReMe)工具则为阿尔茨海默病患者提供个性化训练方案。
面向未来,微软亚洲研究院将持续拓展技术边界,在脑机接口、神经信号识别、无创神经调控等前沿方向积累能力。同时,通过与国内外高校、科研机构及临床医院的深度合作,进一步整合基础研究、临床实践与AI技术的多方优势,让技术创新更紧密地对接真实需求,加速在神经疾病领域的落地与转化,为患者与大众健康创造长期、可持续的价值。
Joint Adaptation of Uni-modal Foundation Models for Multi-modal Alzheimer’s Disease Diagnosis(已被 ICLR 2026 接收)
论文链接:
https://openreview.net/forum?id=gPTjQxC74G
Lab-in-the-loop machine learning for brain-targeting delivery system design(已发表在Cell Biomaterials期刊)
论文链接:
https://www.sciencedirect.com/science/article/pii/S3050562325001217
Personalized progression modelling and prediction in Parkinson’s disease with a novel multi-modal graph approach(已发表在Nature 旗下npj Parkinson’s Disease期刊)
论文链接:
https://www.nature.com/articles/s41531-024-00832-w
#脑科学 #大模型 #人工智能 #神经退行性疾病 #靶向治疗
你也许还想看:


 夜雨聆风
夜雨聆风






