AI重塑ADC设计:当“生物导弹”装上智能引擎
抗体药物偶联物(ADC)被誉为“生物导弹”,通过抗体精准导航将细胞毒性药物送达肿瘤内部。然而,传统ADC开发长期依赖经验筛选和结构生物学,受限于分辨率不足、通量低、组合空间爆炸等问题。如今,人工智能(AI)和机器学习(ML) 正以前所未有的方式渗透进ADC设计的每一个环节——从抗体结构预测、偶联位点优化,到毒素-linker匹配和药代动力学模拟。一篇发表于《Frontiers in Drug Discovery》的综述,系统梳理了这一变革。沿着一条清晰的主线,我们一起看看AI如何为ADC装上“智能引擎”。

第一站:从“手工打磨”到“AI驱动”——一场范式跃迁
早期ADC设计依靠X射线晶体学和分子对接,但抗体柔性区域(如CDR-H3环)和完整IgG结构难以解析。分子动力学模拟虽能提供动态信息,却受限于计算成本和力场精度。
AI/ML的介入彻底改变了游戏规则。深度学习能从海量序列-结构数据中自动提取特征,预测抗体可开发性、优化连接子设计、筛选毒素-抗体组合。如今的ADC设计已从“试错”走向“预测驱动”。
主线一:经验筛选 → AI预测 → 理性设计
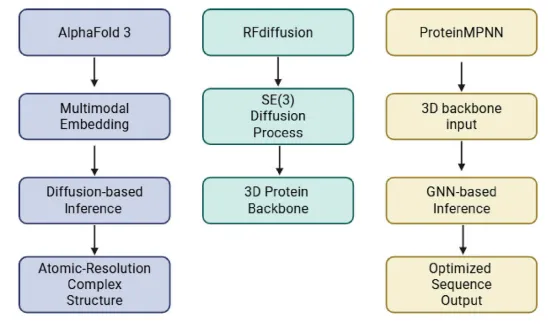
第二站:AlphaFold系列——结构预测的“原子级望远镜”
AlphaFold2实现了单体蛋白的近实验精度预测,但对抗体高变区CDR-H3仍力不从心。AlphaFold-Multimer 开始涉足抗体-抗原复合物,而最新的 AlphaFold3 更进一步:采用扩散生成框架,可同时预测蛋白质、核酸、小分子、离子和糖基化修饰的复合物结构。
对于ADC设计,AlphaFold3能预测Fc结构域的N-糖基化、linker- payload的静态构型,以及抗体-抗原结合表位。虽然仍难以捕捉糖基微异质性和柔性linker的动态行为,但已为ADC的结构建模提供了前所未有的起点。
此外,DeepAb、ABlooper、IgFold 等抗体专用工具,针对CDR环区进行了精细优化,大大提升了建模精度。
主线二:单体结构 → 复合物预测 → 完整ADC建模
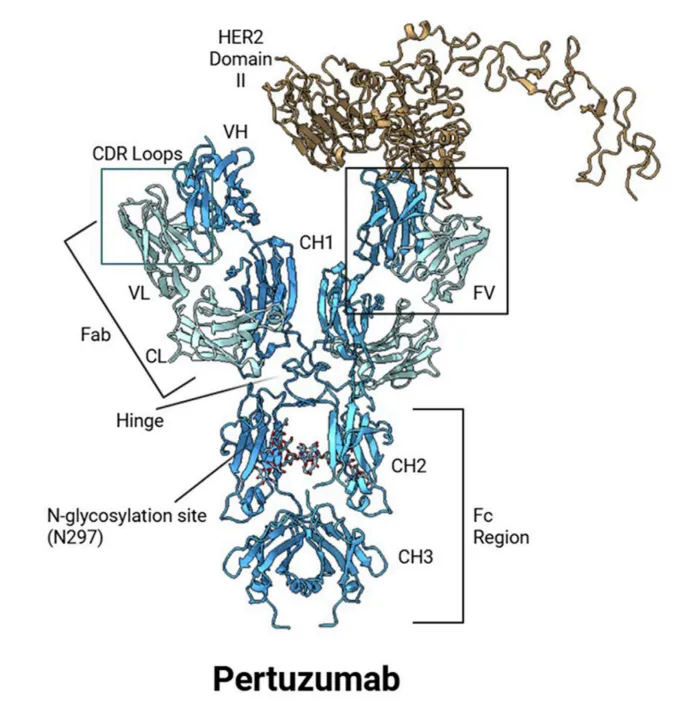
第三站:生成式AI——从“筛选”到“创造”抗体序列
传统抗体亲和力成熟依赖噬菌体展示库筛选,耗时耗力。生成式AI正在改写这一流程:
-
GANs和VAEs:如PALM-H3、Ig-VAE,可生成多样化的CDR-H3序列,在保持结构合理性的同时引入功能多样性。
-
Transformer模型:AntiBERTa、AbLang等预训练模型从抗体序列数据库中学习“语法”,用于预测结构、评分人源化程度、甚至填空修复缺失残基。
-
扩散模型:DiffAb、EvoDiff能直接生成符合特定结构约束(如表位曲率、溶剂可及性)的抗体变体,实现序列与结构的协同设计。
这些工具让ADC开发者能够在计算机中“模拟进化”,快速产出候选分子。
主线三:序列数据库 → 生成模型 → 虚拟抗体库
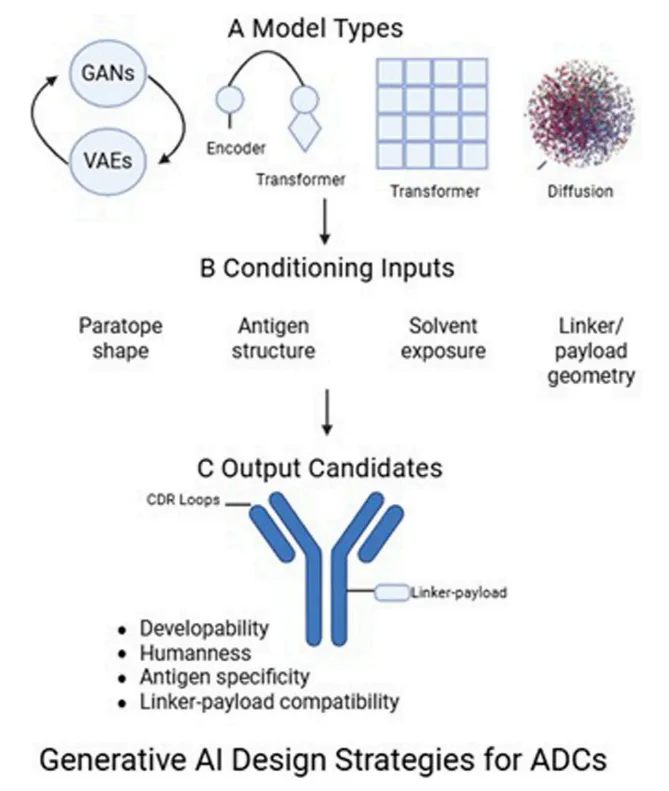
第四站:AI优化linker与ADMET——从“静态”到“动态”
ADC的成功不仅取决于抗体,更依赖 linker-payload 的匹配。AI/ML已被用于:
-
预测DAR(药物-抗体比):ML模型可根据抗体序列和偶联化学,预测最佳药物载量。
-
设计智能linker:结合分子模拟和神经网络,预测linker在血浆中的稳定性、细胞内释放动力学和空间位阻。DiffDock 等扩散模型可模拟linker-抗体- payload三元复合物的结合构象。
-
预测ADMET:集成学习模型可评估ADC的溶解度、聚集倾向、清除率和免疫原性,提前规避后期失败。
特别地,Neural-ODE(如ADCnet) 能连续模拟ADC的内化、linker切割和药物释放的动态过程,捕捉非线性药代动力学行为。
主线四:静态结构 → 动态模拟 → 可开发性预测
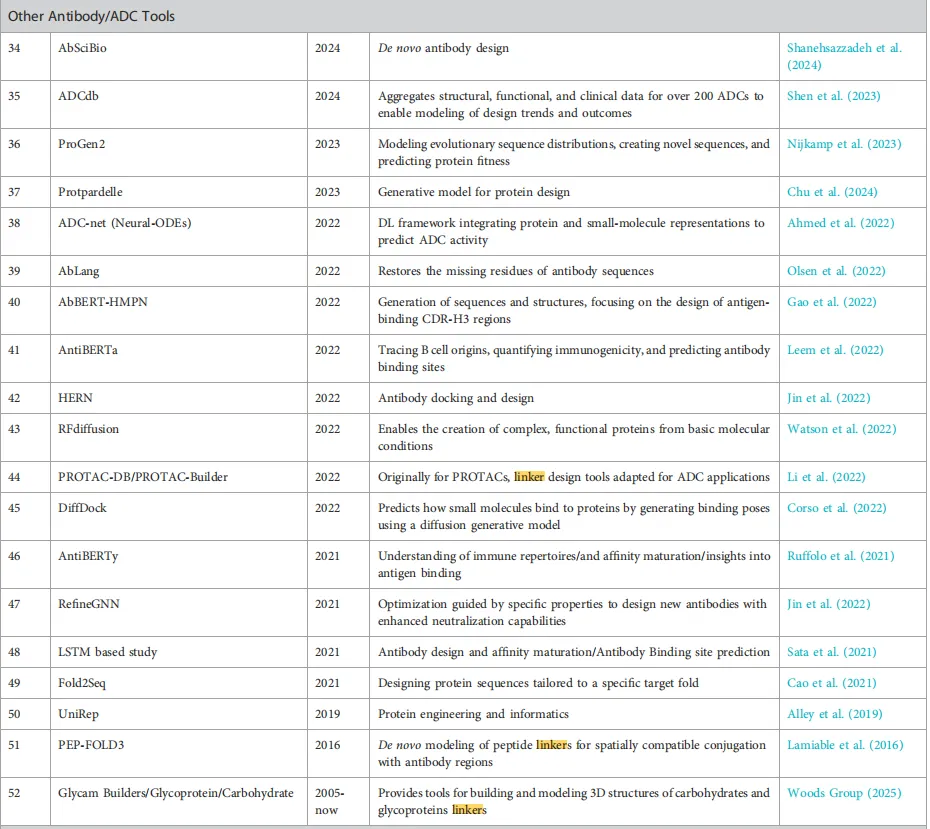
第五站:挑战与未来——AI不是终点,而是桥梁
尽管前景光明,AI-driven ADC设计仍面临几大挑战:
-
数据稀缺:多数ADC专有数据不公开,且标注不一致。迁移学习、数据增强和自监督学习 可在有限数据下提升性能。
-
模型可解释性:黑箱神经网络难以满足监管要求。注意力机制和归因图 可帮助理解模型决策。
-
动态复杂性:ADC的多组分协同效应难以用静态结构描述。未来需整合 多模态数据(结构、组学、临床)和 强化学习闭环,实现“设计-预测-实验-优化”的自动化循环。
展望新一代 多聚体ADC、双特异性ADC和模块化payload系统,AI将不仅限于优化现有分子,更将创造前所未有的复杂构型。
主线五:数据/AI → 预测/验证 → 闭环优化 → 下一代ADC
结语
从结构预测的“原子望远镜”到生成序列的“虚拟进化”,从linker动态模拟到药代动力学建模——AI正在将ADC设计从一门手艺变成一门工程科学。虽然数据、解释性和动态模拟仍需突破,但一个由AI驱动的、可迭代优化的ADC开发新范式已然成形。未来,当“生物导弹”能够通过算法持续自我改进,癌症靶向治疗或将迎来真正的智能时代。
参考文献:Noriega & Wang, Frontiers in Drug Discovery, 2025, 5:1628789
纳米抗体筛选、小鼠单抗筛选、兔单抗筛选、抗体人源化、抗体亲和力成熟、AI抗体设计,欢迎交流咨询。

 夜雨聆风
夜雨聆风




